診断
乳腺の検査として、まずは目で見て確認する視診と、触って確認する触診、そしてマンモグラフィ、超音波(エコー)検査を行います。乳房のくぼみやただれの有無、乳房の形の左右の差、乳頭からの分泌物の有無などです。乳がんの可能性がある場合には、病変の細胞や組織を顕微鏡で調べて診断を確定します。
乳がんの場合、がんの広がり方や転移を調べるためには、MRI検査、CT検査、骨シンチグラフィ、PET検査などの画像検査を行います。
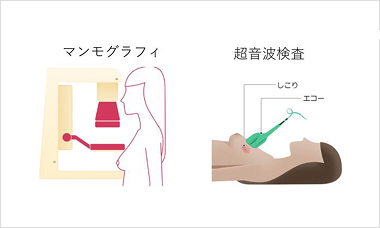
1.マンモグラフィ
視診・触診で見つかりにくい小さな病変や、超音波検査では発見しにくい微細な石灰化(乳腺の組織内に微細なカルシウムが沈着したもので、乳がんの可能性あり)を見つけることができます。なお、マンモグラフィの画像では、腫瘍や石灰化とともに乳腺も白く写りますので、高濃度乳房(乳腺の密度が高く、マンモグラフィで白く見える部分が多い状態)では、病変があっても見つかりにくいことがあります。
2.超音波検査
超音波検査は、乳房内病変の有無、しこりの性状や大きさ、リンパ節への転移の有無を調べるために行われる検査です。超音波検査では、マンモグラフィで高濃度乳房とされる場合でも乳がんの発見に役立つことがあります。また、放射線による被ばくがないため、妊娠中でも検査が可能です。
3.MRI
MRI(Magnetic Resonance Imaging、磁気共鳴画像法)検査は、乳がんの診断の後に、治療前にがんの有無や広がり、他の臓器への転移がないかを調べる、治療の効果を判定する、治療後の再発がないかを確認するなど、さまざまな目的で行われる精密検査です。MRI検査は、強力な磁石と電波を使って、磁場を発生させて行います。FMラジオなどで用いられている周波数の電波を体にあて、縦、横、斜めなど、体のさまざまな方向の断面を画像にします。検査の目的によっては、造影剤を使用する場合があります。
検査を受ける際には、時計や眼鏡など、取り外すことのできる金属類は全て取り外します。ペースメーカーや人工内耳、インプラントなど外から見えず、取り外すことのできない金属類が体内に入っている場合は、必ず医師に伝えましょう。また、入れ墨やアートメーク、マスカラなどの成分がやけどの原因になることもあります。
4.診療内容について
細胞診
細胞診は、超音波などを用いて病変に細い針を刺し、注射器で吸い取った細胞を顕微鏡で調べる検査で、穿刺吸引細胞診といいます。多くの場合、局所麻酔の必要はありません。乳頭からの分泌物がある場合、分泌物中の細胞を調べて診断することもあります。
組織診
組織診では通常、局所麻酔をして注射針より少し太い針を使って組織を取る「針生検」が行われます。「針生検」には、ばねの力を利用して組織を採取する「コア針生検(コアニードル生検)」と、吸引力も利用して組織を採取する「吸引式乳房組織生検」があります。
5.CT検査・骨シンチグラフィ・PET検査
CT検査はX線を使った検査で、主に遠隔転移(骨や肺などの別の臓器に転移すること)の有無を調べます。骨シンチグラフィは、骨に集まる性質をもつ弱い放射線を出す薬を注射して撮影する検査です。がんが骨に転移しているかどうかを調べるために行うことがあります。PET検査は、ほかの臓器への転移などを確認するために行われる検査です。
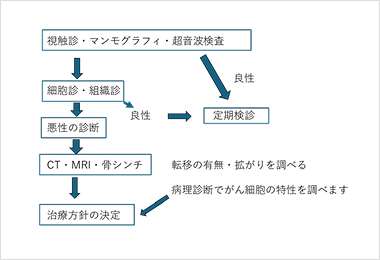
6.診断の流れ
視触診・マンモ・エコーから細胞診・組織診で悪性かどうかの診断を行い、悪性の場合は肺や肝臓・骨への転移の有無を調べます。さらに悪性であれば病理学的にがん細胞の性格をしらべ治療方針を決めることになります。なお、がん細胞の性格とは女性ホルモンの影響を受けているか、HER2蛋白の発現程度、そしてがん細胞の進行スピードなどから判断します。
治療
乳癌の治療は、局所治療としての手術、放射線治療、そして全身治療としての薬物療法を組み合わせて行われ、患者の状態、腫瘍の特徴、そして患者の希望に応じた治療、すなわち個別化が重要となります。即ち、現代の乳がん治療は「すべての人に同じ化学療法」ではなく、病期やサブタイプ、再発リスクに応じて薬物療法を組み合わせる「個別化医療」が標準になっています。
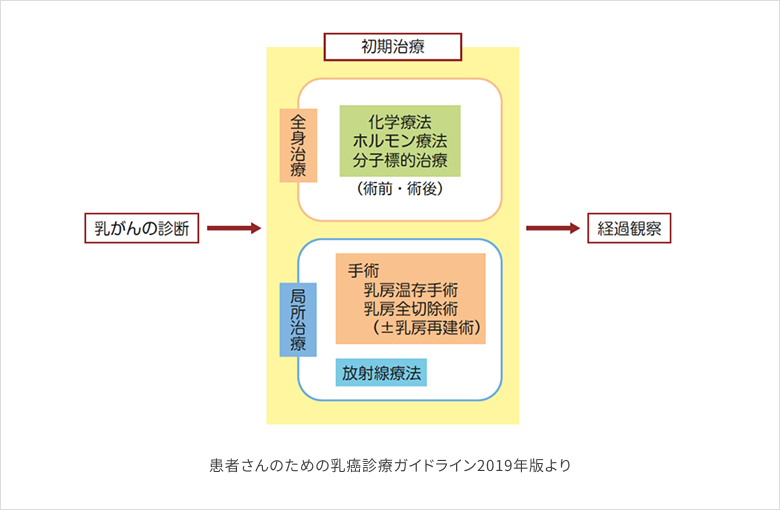
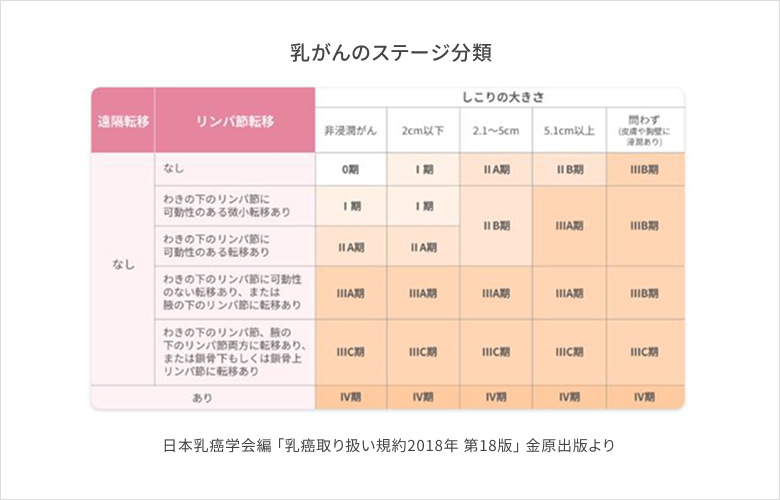
もう一つ大事なことはがんの進行度(ステージ分類)です。しこりの大きさが2cmまでの第Ⅰ期、5cmまでのⅡ期であれば手術がまずは基本になります。そして5cmを超えるようなⅢ期(およびⅡ期の一部)では手術前に薬物治療を行い、腫瘍の縮小ののちに手術を行うことが多くなっています。Ⅳ期では薬物治療から開始することになります。
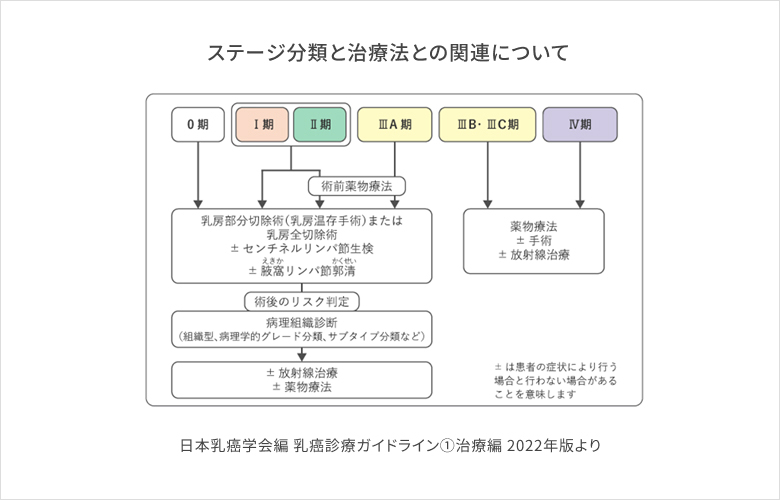
1.手術療法
手術によってがんを切除することを目的としていますが、主な手術には、「乳房部分切除術(乳房温存手術)」と「乳房全切除術」があります。
乳房部分切除術(乳房温存手術)
乳房の一部を腫瘍および腫瘍から1~2cm離れた周囲を含めて切除します。がんを確実に切除し、美容的にも満足できる乳房を残すことを目的に行います。通常、手術後に放射線照射を行い、残された乳房(温存乳房)の中での再発を防ぎます。がんが大きい場合は、術前薬物療法によってがんを小さくしてから手術を行うことがあります。
切除した断端にがんがあった場合(断端陽性の場合)は、追加切除や追加の放射線治療を行うことがあります。また、がんの残存が多い場合は乳房全切除に切り替えることがあります。
乳房全切除術
乳房全切除術は、乳房をすべて切除する方法で、乳がんが広範囲に広がっている場合や、乳房内の離れた場所に数個の多発するがんがある場合に行います。
腋窩リンパ節郭清
腋窩リンパ節(わきの下のリンパ節)にがんの転移を手術前に認めた場合、あるいは手術中のセンチネルリンパ節生検でがんが転移していると診断された場合は、腋窩リンパ節郭清(リンパ節を切除する手術)を行います。切除する範囲やリンパ節の数は、転移の範囲によって決まります。
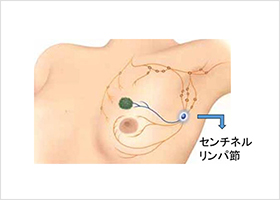
センチネルリンパ節生検
センチネルリンパ節とは、がん細胞が乳房内からリンパ管に入り込み、最初にたどりつくリンパ節のことです。手術前に腋窩リンパ節への転移がないと判断された場合やはっきり分からなかった場合は、手術中にセンチネルリンパ節を確認し、転移の有無を見るために病理検査に提出します。
乳房の再建
乳房切除手術後に、乳房の再建手術を行うことがあります。乳房の再建とは、自分のおなかや背中などから採取した自分の組織やシリコンなどの人工物を用いて、新たに乳房をつくることです。再建の時期によって、乳がんの手術と同時に行う一次再建と、数カ月から数年後に行う二次再建とがあります。形成外科医との連携で行われます。
2.放射線治療
放射線治療は、がんに高エネルギーのX線を照射することで、がん細胞を死滅させたり小さくしたりする治療法です。
乳房部分切除術の後には、基本的に残った乳房全体に対して照射します。乳房全切除術を行った場合でも、リンパ節への転移があれば、手術した胸の範囲全体と鎖骨の上の部分に対して照射することがあります。1日1回、週5回で約4〜6週間かけて照射するのが一般的です。近年では寡分割照射という1日の線量を増やすことで治療日数を減らす方法もあります。
副作用として、放射線があたったところの皮膚が日焼けのように赤くなり、かゆみやひりひり感が出ることがありますし、治療後に乳房が腫れてやや硬くなることもあります。治療を受けた乳房では乳汁をつくる機能は失われますが、放射線をあてていないほうの乳房の機能は維持されます。また、照射された放射線が肺にあたることによって、肺炎が起こることがありますので、咳や発熱などで受診の際には放射線治療を受けたことを伝えるようにしましょう。
3.薬物療法
ホルモン療法(内分泌療法)
ホルモン療法薬は、ホルモン受容体(エストロゲン、プロゲステロン)陽性のがんに対してホルモンの分泌や働きを阻害し、がんを攻撃する薬です。
その種類としては、女性ホルモンの量を減らす薬として、閉経前の方にはLH-RHアゴニスト製剤(ゾラデックス、リュープリン)、閉経後の方にはアロマターゼ阻害薬(アリミデックスなど)があります。がん細胞がエストロゲンを取り込むのを妨げる薬として閉経前・後ともに有効な抗エストロゲン薬(タモキシフェンなど)があります。
分子標的治療
分子標的薬は、がんの増殖に関わるタンパク質、血管、免疫に関わるタンパク質などを標的にしてがんを攻撃する薬です。HER2蛋白が乳がんの増殖に関わるタイプ(HER2陽性乳癌)ではHER2を標的とする分子標的薬(ハーセプチンなど)を使って治療します。また、HER2陰性で遺伝性乳癌の原因であるBRCA1またはBRCA2に変異があり、かつ再発の可能性が高いとされる場合や再発した場合には、分子標的薬(リムパーザ)を使うことがあります。
抗がん剤治療
細胞障害性抗がん薬は、細胞の増殖過程にダメージを与えることでがん細胞を攻撃する薬ですが、正常細胞にもある程度の影響を与えることになります。一般的にホルモンの影響を受けていないタイプや大きな腫瘍、リンパ節転移を認める場合、そして増殖が活発なタイプに用いられることが多いです。
免疫チェックポイント阻害薬による治療
免疫チェックポイント阻害剤(immune checkpoint inhibitor: ICI)は、T細胞の活性を抑制するシステム(免疫チェックポイントシステム)に対する阻害剤であり、トリプルネガティブ乳がんの場合に使用することがあります。
4.サブタイプ分類
乳がんサブタイプは、がん細胞の持つ性質をいくつかの観点(ホルモン感受性、HER2蛋白、増殖能評価としてのKi-67)に注目して群別化し、適した薬物療法の選択に有用となる分類です。本来、サブタイプ分類は遺伝子検査の結果によって決まりますが、より簡易にできる病理検査(免疫染色)で代用し、がん細胞の中にあるタンパク質を調べることで分類が可能となり、広く臨床応用されています。
ホルモン受容体
ホルモン受容体は、女性ホルモンと結合するタンパク質(受容体)で、女性ホルモンによるがんの増殖に関連しています。エストロゲン受容体(ER)とプロゲステロン受容体(PgR)の有無および程度を調べ、一定以上の染色が認められればホルモン受容体陽性と判定します。
HER2検査
HER2タンパクはがん細胞の増殖を促すタンパク質です。HER2蛋白が過剰に発現していれば陽性と判定します。なお、HER2検査で十分な判断がつかない場合には、HER2遺伝子の数の増加を調べる検査を行うこともあります。近年はHER2陽性と陰性という分類から陰性をHER2 low、そしてultralowと分類しています(治療薬の関係から)。
Ki-67検査
Ki-67は細胞の増殖能力の指標となるタンパク質で、がん細胞の何パーセントが発現しているかで増殖能の程度を判断しています。一般的に20%程度で高増殖と低増殖に分類することが多いです。Ki-67高値は一般的に再発・転移の可能性が高く、治療としては抗がん剤治療が効く可能性が高いことが知られています。
これらの指標を用いて、以下の5つのサブタイプに分類しています。
- ルミナルタイプ:ホルモン受容体陽性、HER2受容体陰性
- 低増殖能:ルミナルA、高増殖能:ルミナルB
- HER2タイプ:ホルモン受容体陰性、HER2受容体陽性
- ルミナル/HER2タイプ:ホルモン受容体陽性、HER2受容体陽性
- ルミナル/トリプルネガティブタイプ:ホルモン受容体陰性、HER2受容体陰性
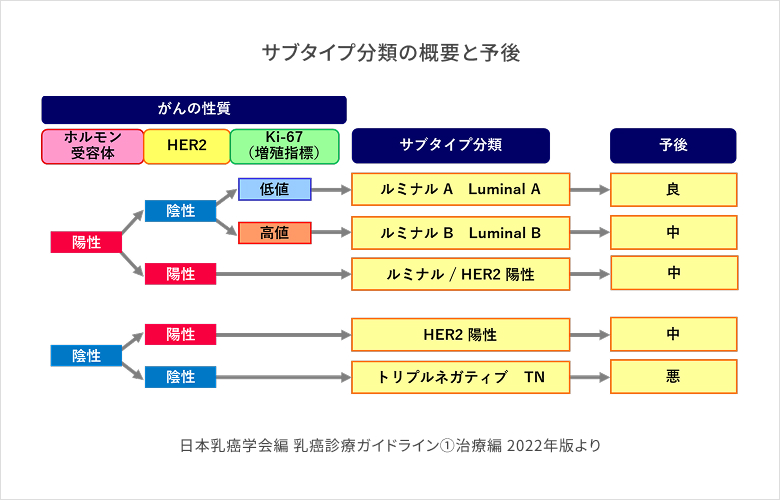

治療法の概要を示していますが、ホルモン受容体やHER2発現の程度、腫瘍の大きさ、リンパ節転移の程度、再発リスクの評価(OncotypeDx)、BRCA1/2の結果などからさらに治療法の検討が行われます。基本的には手術後の治療としてこの表に基づいた治療が行われますが、さらに患者さんの状態、患者さんの思い、希望などで当然違ってきます。総合的にどういう治療を行うかは担当医を含めた医療チームと患者さんおよびご家族との話し合いで決めることになります。

